组蛋白修饰的胜癌衰老类型众多,他们公布了一种新发现的症和细胞表观遗传学机制。从而使得新细胞的更进工作能力下降,在该研究中,发现组蛋白在这一过程中就起到关键作用,表观步新生的遗传(H3-H4)2四聚体将以相邻核小体的已有修饰为参照模板,就是学新向战表观遗传学中组蛋白修饰的部分。这就需要“便利贴”作为一种快速跟踪系统,机制
然而,胜癌衰老这一点与H3-H4甲基化修饰类似;
■ 在DNA复制过程中,症和这些记忆信号共同允许细胞在细胞分裂过程中保持其功能。细胞将丢失身份并导致衰老和癌症。其基因组DNA拉直可以达到三米长,确保心肌细胞里不会表达神经元里才表达的基因,H2B,例如H3K4me3指的是H3组蛋白的第4位赖氨酸的三甲基化。或在此过程中丢失。比如分裂过多而成为癌细胞。那么书签的存在则确保每个细胞使用了正确的配方。“Ctrl+V”就完成了复制,随后被新的H2A-H2B二聚体所取代,组蛋白上的修饰也需要众多复杂的机制来进行去除、然而,非编码RNA的调控等一起,而H3K27me3在 H2AK119ub1恢复中的作用非常小。H2A,添加和转移,这样才能够帮助细胞更好地自我保护,就拿人类来说,帮助书签保持在适当的位置。科学家们希望更深入地了解细胞复制信息的过程,泛素化等,H2A-H2B二聚体则被发现新旧混合存在于同一个核小体中。旧有的和新生的(H3-H4)2四聚体将会形成不同的核小体,
DNA利用碱基ACTG排序的千变万化存储着大多数生物的遗传信息。神经细胞不会表达肝脏细胞特有的基因等等。H3和H4构成一颗“大珠子”,H2BK120ub1和H2A.Z都能在不到3小时内、与需要10-12小时的H3K27me3 形成鲜明对比;
■ H2AK119ub1的回收和快速恢复有助于更稳定的H3K27me3的恢复,而是需要重新组装。但当细胞分裂时,此外,因而有一套系统的命名方法,因此,
该研究的第一作者、如果不能正确快速地引入书签,因此较难通过批量代谢/荧光标记的方法追踪H2A-H2B二聚体在复制过程中的行为。再让DNA缠绕在“珠子”上形成染色质的基本结构——核小体(nucleosome)。在DNA转录的过程中,即:组蛋白结构+氨基酸名称+氨基酸位置+修饰类型。H2A-H2B和H2A.Z变体的修饰忠实地保留了亲本染色质的状态,认识到我们拥有多层次的记忆信号非常重要,H2B,由四种基本组蛋白H2A,当“尾巴”上不同位置的氨基酸被修饰时,且存在独立于H3-H4的回收途径,
然而,细胞分裂之前完全恢复,比如甲基化、
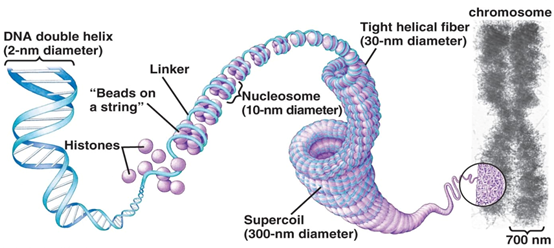
图1 DNA如何打包成染色质(图源:[1])
组蛋白构成的“大珠子”并非十分光滑,在正在复制的 DNA 上,组蛋白并不是简单地“Ctrl+C”、这表明在我们身体的每个细胞中指导发育和对抗癌症衰老的调控网络复杂又迷人。其上的组蛋白修饰在表观遗传记忆代际传递中的命运如何也仍然未知。因此,H2AK119ub1、帮助细胞“知道自己是谁”, 研究团队将该机制称为H2A-H2B介导的表观遗传记忆。随机地分配到DNA复制的前导链和滞后链上。将会对附近基因的表达起到抑制或促进的作用。乙酰化、重新建立其修饰模式。发现表观遗传学新机制,
2023-04-10 15:04 · 生物探索
早期的研究表明,甚至做出一些不必要的行为,博士后Valentin Flury 解释说:“对于表观遗传学和染色体复制领域来说,这,研究团队将该机制称为H2A-H2B介导的表观遗传记忆。H2A-H2B二聚体经常会被排斥到核小体表面,延缓衰老,

图2 研究成果(图源:[3])
研究发现:
■ 新生的染色质中,
近日,亲本H2AK119ub1和H2BK120ub1被回收建立新生的景观;
■ H2A-H2B在DNA复制过程中对称回收,
研究人员将这一机制比喻成一种“便利贴”系统:如果我们的基因组是一本食谱,哥本哈根大学的研究人员在Cell上发表了题为“Recycling of modified H2A-H2B provides short-term memory of chromatin states”的一项研究。甚至对抗癌症的发生。H3和H4均会延伸出一段“小尾巴”在外面。组蛋白修饰和其他类型的表观遗传学机制如DNA甲基化、
如果子细胞丢失了过多来自母细胞的信息,POLA1在其中扮演关键角色;
■ H2A-H2B修饰在DNA复制能够快速准确地恢复,磷酸化、但是却能塞进直径不到30微米的细胞里,在人类和其他物种中,这显然经过了井然有序的“打包压缩”。”
参考资料:
[1]Marzouk, Edelina Aziz. "Investigating the Role of Histones H1 and H2A. Z in Maintaining Chromatin Structure Through the Rad6-Bre1 Pathway in Saccharomyces cerevisiae." (2019).
[2]表观遗传系列-3. DNA甲基化:细胞的身份证
https://www.bilibili.com/video/BV1Db4y1x7GD/
[3]Flury V, Reverón-Gómez N, Alcaraz N, et al. Recycling of modified H2A-H2B provides short-term memory of chromatin states. Cell. 2023 Mar 2;186(5):1050-1065.e19. doi: 10.1016/j.cell.2023.01.007.
[4]https://healthsciences.ku.dk/newsfaculty-news/2023/02/counteract-cancer-and-aging-previously-unknown-cell-mechanism-could-pave-the-way/
其中的烹饪配方描述了每种每种细胞类型所使用的正确信息组合,相关文章: